英文特生物技术(北京)有限公司品牌商
11 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
推荐产品
公司新闻/正文
一文了解蛋白亚细胞定位研究!
1352 人阅读发布时间:2025-08-05 11:38

蛋白亚细胞定位(Protein Subcellular Localization) 是指蛋白质在细胞内的特定区域或细胞器中的空间分布状态。这些区域包括细胞核、细胞质、线粒体、内质网、高尔基体、溶酶体、过氧化物酶体、细胞膜、细胞骨架(如微管、微丝)或分泌到细胞外等。

“蛋白质通过其自身携带的‘地址码’(信号序列/结构域),被细胞内的‘物流系统’(转运机制)精准投递到特定细胞器或区域,并在该空间内执行功能。”
其原理可拆解为四个核心环节(从合成到驻留):信号序列-转运机制-动态调控-驻留信号四步协同
1. 地址编码:信号序列决定目的地
-
核定位信号(NLS):如SV40大T抗原的 PKKKRKV,被核转运受体(importin-α/β)识别,介导核孔复合体(NPC)转运。
-
线粒体靶向序列(MTS):N端带正电的两亲性α螺旋(如细胞色素c氧化酶亚基IV),被TOM/TIM复合体识别。
-
内质网信号肽:N端疏水序列(如胰岛素前体的MALWMRLLPLLALLALWGPDPAA),由SRP引导至ER膜。
-
过氧化物酶体定位信号(PTS1/2):C端SKL三肽或N端九肽,被PEX5/PEX7受体识别。
例外:无信号序列的蛋白可通过“搭便车”(结合已定位的伴侣蛋白,如14-3-3)或被动扩散(小蛋白如组蛋白H1)。
2. 转运机制:分子物流系统
-
核孔运输:通过NPC的“选择性门控”机制,大分子需核转运受体(如importin/exportin)+Ran-GTP梯度驱动。
-
囊泡运输:COPII(ER→高尔基体)、COPI(反向回收)、网格蛋白(质膜内吞)。
-
膜嵌入:线粒体/叶绿体的TOM/TIM或TOC/TIC复合体,通过电化学梯度或ATP水解将蛋白拉入基质。
-
细胞骨架马达:驱动蛋白(kinesin,顺微管正向运输)、动力蛋白(dynein,逆向运输)、肌球蛋白(微丝运输)。
3. 动态调控:定位的“可塑性”
-
翻译后修饰(PTM):
-
-
磷酸化:如转录因子STAT3被JAK磷酸化后暴露NLS,触发核输入。
-
泛素化:膜蛋白被泛素标记后经ESCRT复合体分选至溶酶体降解。
-
-
蛋白质互作:
-
-
14-3-3蛋白通过结合磷酸化位点“扣押”FOXO转录因子于胞质,阻止其入核。
-
-
细胞器应激:
-
-
内质网未折叠蛋白反应(UPR)时,ATF6被切割后N端片段转入核内激活应激基因。
-
4. 驻留与回收:防止“迷路”
-
驻留信号:
-
-
内质网驻留信号KDEL(如BiP蛋白),被KDEL受体识别并回收。
-
核仁驻留通过NPM1等支架蛋白的RNA结合域维持。
-
-
质量监控:
-
-
错误定位的蛋白被细胞器表面泛素连接酶(如线粒体MUL1)标记,经蛋白酶体降解。
-

“知其所在,知其所以用,知其所以病,知其所以治” 是研究蛋白亚细胞定位的重要意义。
1. 知其所在:定位决定功能
蛋白质的功能与其所处的微环境(细胞器、膜系统、复合体)直接绑定。
-
核内的p53是转录因子,调控细胞周期;若滞留胞质,则丧失抑癌活性。
-
线粒体膜间隙的细胞色素c是电子传递链组分,释放到胞质则触发凋亡。
-
突触前膜的SNARE复合体介导神经递质释放,若错误定位至胞体则导致神经信号障碍。
2. 知其所以用:指导合成生物学与代谢工程
-
代谢通路优化:将乙醇合成途径的酶靶向过氧化物酶体,避免中间产物毒性积累(如甲醇利用酵母)。
-
药物递送:设计线粒体靶向抗氧化剂(MitoQ)治疗帕金森病,需依赖MTS信号引导。
-
人工细胞器构建:通过融合定位信号(如PEX靶向序列),将非天然酶“安装”到特定区室,实现功能隔离。
3. 知其所以病:蛋白定位异常是疾病的“分子指纹”
|
疾病类型 |
定位异常案例 |
机制与后果 |
|
癌症 |
β-catenin核积累 |
E-cadherin膜定位丧失→Wnt通路过度激活→转移 |
|
神经退行性疾病 |
TDP-43从核内错误定位到胞质应激颗粒 |
抑制RNA剪接→神经元死亡(ALS/FTD) |
|
囊性纤维化 |
CFTR的ΔF508突变导致ER滞留 |
无法到达膜表面→氯离子通道功能缺陷 |
|
感染 |
病毒蛋白(如HIV Rev)劫持核输出通路(CRM1) |
病毒mRNA逃逸核内监控→高效复制 |
意义:定位异常可作为早期诊断标志物(如前列腺癌中PCA3的核仁富集)。
4. 知其所以治:靶向定位的精准干预策略
-
恢复定位:小分子伴侣(如lumacaftor)帮助ΔF508-CFTR折叠并转运至膜,治疗囊性纤维化。
-
阻断错误定位:CRM1抑制剂(selinexor)阻止肿瘤抑制蛋白(如p53)的核输出,增强化疗敏感性。
-
人工调控:光控核定位系统(如LOV2-NES)实现时空特异性基因编辑(CRISPR-dCas9的核输入开关)。

亚细胞定位的研究方法可分为实验验证和计算预测两大类。
一、实验验证方法(目前主流)
1. 荧光蛋白融合法(GFP/eYFP/mCherry)
-
原理:将目标蛋白与荧光蛋白融合表达,利用共聚焦显微镜观察。
-
适用系统:
-
-
植物:烟草瞬时表达(农杆菌介导)
-
动物:293T细胞、HeLa细胞瞬时转染或稳定表达
-
-
优势:活细胞实时观察,直观、灵敏
-
注意事项:
-
-
需设置细胞器Marker(如mCherry标记线粒体、核、膜等)
-
避免过表达引起的定位假象
-
2. 亚细胞组分分离 + Western Blot
-
原理:通过细胞组分分离(Cell Fractionation)获得不同亚细胞结构(如细胞核、细胞质、细胞膜、细胞器等),检测目标蛋白在各组分中的分布。
-
亚细胞组分分离方法 :Invent柱式法Minute TM系列亚细胞结构组分分离工具,可分离细胞质、细胞膜、细胞核、线粒体、溶酶体,内质网,高尔基体,染色质等多种亚细胞结构。无需超高速离心,无需自配溶液,仅需台式离心机,1小时左右即可完成亚细胞组分分离。
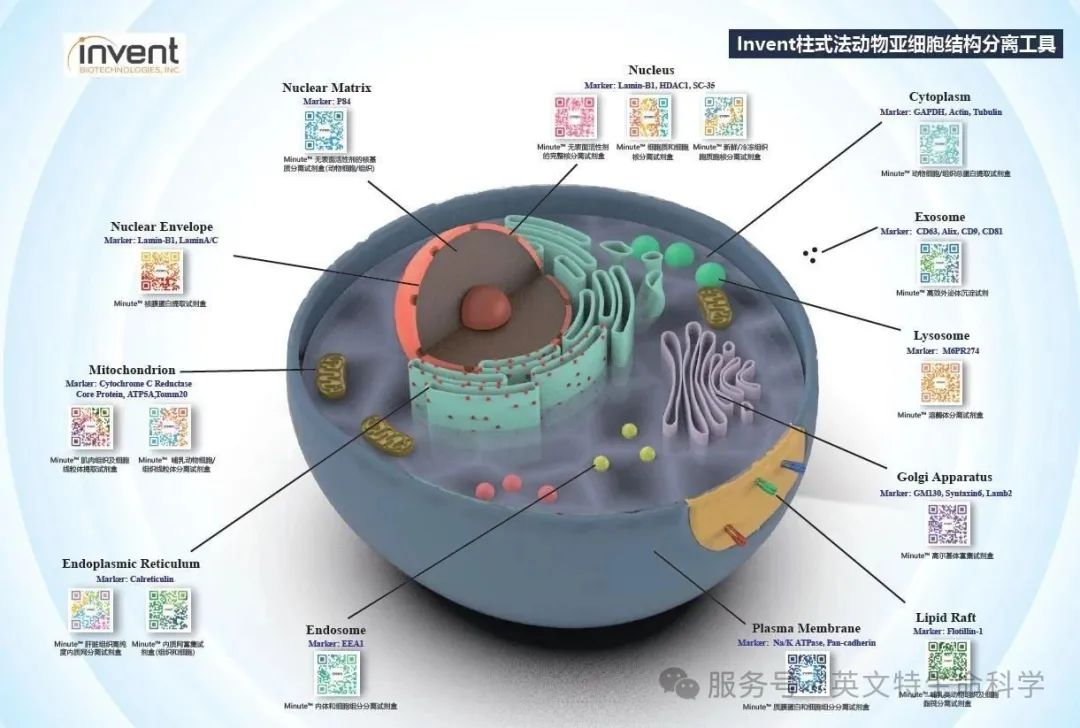
-
适用:验证荧光结果,适合蛋白组学分析
案例分享
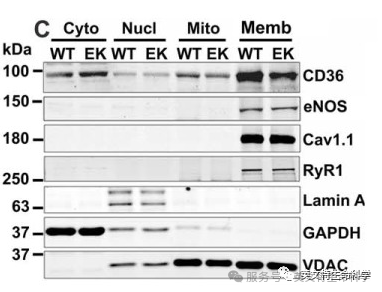
图片来源:doi:10.1074/jbc.M115.643544 jbc.M115.643544.
Georgiou等人研究钙离子通道复合物Cav1.1调控脂肪酸转运蛋白CD36分布和脂肪酸代谢。Cav1.1 E1014K基因敲除小鼠(EK)和野生小鼠(WT)的肌肉组织样品,使用离心管柱法进行细胞组分分离,分离后的细胞浆,细胞核,细胞膜以及线粒体组分进行Western Blot,检测CD36的表达及分布情况。Lamin A, GAPDH, 及VDAC 分别为细胞核,细胞浆及线粒体组分的内参。结果表明,与WT相比,EK小鼠的CD36在细胞浆组分定位增加,在质膜组分定位减少。其它膜蛋白(eNOS,Cav1.1,RyR1)则无明显变化。
3. 免疫荧光染色(IF)
-
原理:使用特异性抗体标记内源蛋白,适用于固定细胞。
-
优势:无需构建融合蛋白,可用于内源蛋白
-
工具:DAPI染核、共聚焦显微镜成像
4. 稳定转化系统
-
原理:将融合蛋白整合到基因组中,长期稳定表达。
-
应用:植物转基因株系(如水稻、拟南芥)用于组织特异性定位
二、计算预测方法(辅助)
|
方法 |
工具示例 |
输入 |
输出 |
|
序列预测 |
DeepLoc、WoLF PSORT |
蛋白质氨基酸序列 |
预测细胞器定位 |
|
结构预测 |
AlphaFold3 |
蛋白结构 |
推断可能定位区域 |
|
多模态融合 |
图像+质谱联合建模 |
免疫荧光+AP-MS |
构建亚细胞蛋白图谱 |