英文特生物技术(北京)有限公司品牌商
12 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 1.2999999999999998
- 0.2999999999999998
推荐产品
公司新闻/正文
膜蛋白WB技巧
4018 人阅读发布时间:2024-04-17 11:24
膜蛋白WB相对于其他蛋白更加困难,主要原因有:
1)部分膜蛋白表达量较低,在总蛋白中占比低不易检测;
2)膜蛋白结构复杂,特别是跨膜蛋白,不易被提取;
3)膜蛋白有很多属于大分子量蛋白,比起小分子量蛋白,提取和转膜更加困难。
基于以上原因,我们将从提高膜蛋白提取效率及提高大分子量蛋白WB检出效率两点出发,快速攻破膜蛋白WB困境。
提高膜蛋白提取效率
了解膜蛋白结构及表达情况
通过生信信息,查询了解目标膜蛋白在哪些组织中表达,是否具有特异性,是否是跨膜蛋白,跨了几次膜,以及蛋白质的分子量大小和表达量如何。这些信息可以帮助我们初步判断目标膜蛋白提取的难易程度及应该使用哪种制备方案。
判断方法案例:
(1)目标膜蛋白表达量较好,且不属于跨膜蛋白,可以优先选择总蛋白提取检测。
(2)目标膜蛋白表达量比较低时,每条泳道可加入的蛋白总量是有限的,使用总蛋白检测时就限制了这些低丰度蛋白的检测。因此,最好需要预先富集膜蛋白,才更容易检出。
(3)目标蛋白跨膜次数越多,提取的难度相对越大,也最好预先富集膜蛋白后再检测。
(4)动物组织样本裂解难度大于培养的细胞样本,选用裂解液提取动物组织样本总蛋白时,要优先选用对膜蛋白提取效率更好的方法。
选择合适的膜蛋白制备方案
膜蛋白WB样品制备有两种方案可选,一种为常规总蛋白制备方案,另一种为富集膜蛋白方案。
常规总蛋白制备方案:
总蛋白提取是通过对组织或细胞样品进行裂解,释放出目的蛋白。不同的裂解液配方对蛋白溶解能力有所不同。基于溶液法的提取裂解液有RIPA,NP-40,Triton X-100,SDS等。最常用的RIPA裂解液,经过离心后可获取可溶性蛋白上清,而沉淀中则含有很多不可溶组分(胞膜,细胞器,核酸,不可溶性蛋白),因此对膜蛋白的提取效率低,且已被证实有 10-30% 的蛋白会丢失在不可溶组分中,影响蛋白的提取质量及完整性【1,2】,并缺少有效的杂质去除步骤,获得的蛋白纯度较低。因此并不建议使用RIPA裂解液进行膜蛋白的提取。
推荐使用升级方案,Invent柱式法总蛋白提取试剂盒(Cat#SD-001/SN-002)进行无内源基线改变的总蛋白提取,柱式法采用离心管柱技术和优化的裂解液配方,蛋白提取过程不产生不可溶性的沉淀,可更为有效的提取膜蛋白,改善因RIPA不可溶造成的蛋白丢失问题。离心管柱同时可有效去除核酸及碎片干扰,进一步提高蛋白样品质量和纯度。
Fig1.柱式法SD-001裂解液与RIPA裂解液裂解效率对比图
富集膜蛋白方案:
传统富集膜蛋白采用密度梯度离心法,通过蔗糖密度梯度离心来完成膜的亚细胞结构分级分离,通常被用来富集不同的细胞器和细胞膜。但是样品需求量巨大,得率较低,需要使用超高速离心机和自配密度剂,操作时间长步骤繁琐,提取的细胞膜成分经常受到其他细胞器膜的污染,特别是线粒体、内质网、高尔基体膜等污染。为打破传统膜蛋白获取方法的局限性,推荐使用新一代膜蛋白分离技术——Invent柱式法亚细胞结构分离工具。例如Invent质膜和细胞组分分离试剂盒(Cat#SM-005),利用离心管柱技术,无需超高速离心机,即可以获取具有天然活性,且与细胞器交叉污染极低的质膜结构,可用于各类下游检测。分离原理:细胞/组织通过Buffer A致敏,在16000Xg离心作用下细胞通过离心管柱(Z字形通道),细胞膜被划开使得细胞破裂,后续通过差速离心和密度离心将依次得到细胞核、胞浆、细胞器以及质膜四个组分,均可用于下游检测。
Fig2.SM-005质膜和细胞组分分离试剂盒分离原理示意图
提高大分子蛋白WB检出效率
蛋白制样
膜蛋白具有疏水性,当它们在高温下煮沸时,倾向于聚集并形成二聚体或多聚体,不能被抗体很好识别。此外,大的聚集体还可能直接沉淀,即使放入凝胶孔中,也可能滞留在胶孔中,从而导致随后的检测失败。因此,热变性温度对膜蛋白检测的影响极大,建议采用37℃,孵育30分钟,或者根据样品本身情况,采用梯度温度热变性检测最佳温度后,谨慎调整热变性温度,以提高检测效率。
分离胶的使用及浓度
凝胶主要有Tris-Glycine, Bis-Tris and Tris-Acetate三种,Tris-Glycine凝胶的pH为8.6,Bis-Tris凝胶的pH为6.4,Tris-Acetate 凝胶的pH为7。推荐使用Tris-Acetate 凝胶跑大分子蛋白,会呈现更高的分辨率。凝胶浓度与孔径成反比,即凝胶浓度越小,孔越大,较大分子量的蛋白质更容易通过,所以建议使用6-8%浓度的分离胶,当然也可以使用梯度凝胶。
经过小编的阅读查找,为大家找到了详细的参考资料以及Tris-Acetate 凝胶3-15%的梯度胶配方。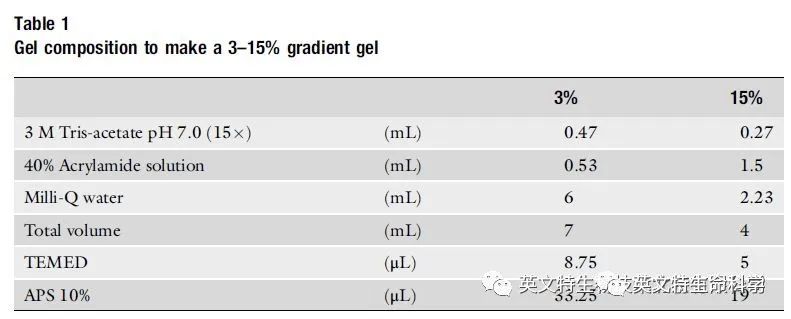
电泳
电泳时,可采用120-150V的高电压,在冰水浴中进行,尽量使Marker拉开足够大的距离,通常需要4小时左右。
一些经验值:师兄A:120V电压,4小时,245KDa Marker条带差不多到分离胶中间位置。
转膜
转印膜的选择
大分子量蛋白,一般建议使用0.45um的PVDF膜。
切胶
浓缩胶不要切得太过,因为很有可能条带就在浓缩胶和分离胶交界以下2mm处(还有可能许多分子量超过250KDa的蛋白就残留在浓缩胶中)。
Transfer buffer
Transfer buffer中的甲醇容易让大分子量蛋白沉淀,所以减少Transfer buffer中甲醇百分比(10%或更低)来避免这种情况发生,并添加SDS至终浓度为0.1%,进一步确保蛋白质不会沉淀。
转膜
湿转法与半干转法均可(湿转获得条带更好,半干转转膜效率高)
湿转法,以下是师兄B摸索出来转膜时间(仅供参考) 
半干转,以下是师兄C摸索出来转膜条件(仅供参考)
恒压40V电压,转膜60-90min,一般小于400KDa的蛋白都能转到PVDF膜上。恒流法转,电流大小设置为PVDF膜的面积,转1小时左右即可,若怕转膜过头,可以将两张PVDF膜重叠起来(总会有一张膜上有条带)。
其他注意事项
1.强烈建议转膜后,使用丽春红染液染膜(Invent Cat# WA-004),检验转膜效率,蛋白条带分布和上样量如何,如果染色后无条带,则需考虑样品问题及转膜问题,进行调整。(丽春红染色怎么做点这里)
2.大分子蛋白与PVDF膜的结合不是很牢固,容易脱落,洗膜时要操作轻柔,不要过于粗暴,否则抗原抗体复合物容易脱落。
小结
膜蛋白WB检测难度高,选择合适的蛋白制备方案,提高样品中膜蛋白的含量是重中之重,控制膜蛋白热变性温度,优化大分子量膜蛋白电泳与转膜条件,膜蛋白WB检测将不再成为我们的“痛点”!预祝大家实验成功~
参考文献:
1.Kevin A. Janes,2017,Sci Signal. ; 8(371): rs2. doi:10.1126/scisignal.2005966.
2.Li Q,et al.(2016). Pitfalls of Protein Extraction by RIPA Buffer. BioTechniques 61:327 .doi 10.2144/000114486